-
 华东医药注射用醋酸卡泊芬净获批上市
华东医药注射用醋酸卡泊芬净获批上市国家药监局官网显示,华东医药子公司杭州中美华东制药的注射用醋酸卡泊芬净获批上市。米内网数据显示,近年中国公立医疗机构终端卡泊芬净注射剂销售额2019年突破20亿元,其中,默沙东市场份额占比最大。截至目前,注射用醋酸卡泊芬净共有5家国产生产厂家,今年以来,已有信泰制药(苏州)、辽宁海思科制药、杭州中美华东制药三家获批。
2020-11-24 来源:米内网 -

-
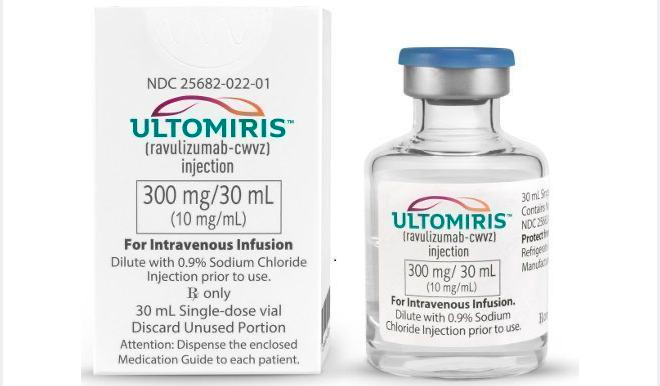 欧盟批准Ultomiris 100mg/mL高浓度制剂:输液时间将减少60%
欧盟批准Ultomiris 100mg/mL高浓度制剂:输液时间将减少60%在美国,Ultomiris 100mg/mL IV制剂于今年10月获得批准:(1)治疗PNH成人患者;(2)治疗aHUS成人和儿童(≥1个月)患者,以抑制补体介导的血栓性微血管病(TMA),Ultomiris 100mg/mL制剂可减少约60%的平均年输液时间,同时具有可比的安全性和有效性。
2020-11-23 来源:生物谷 -
 第四批集采名单预测,涉及73个产品
第四批集采名单预测,涉及73个产品从“4+7”集采到集采扩围、第二批、第三批……不到两年的时间里,已进行了三批四轮国家药品集中采购。当第四批药品集采也呼之欲出,集采常态化已成为共识。
2020-11-20 来源:E药经理人 -
 国内外疫苗产业发展现状分析研究
国内外疫苗产业发展现状分析研究根据《EvaluatePharma WorldPreview 2020》披露,2019年全球疫苗市场规模约325亿美元,在所有治疗领域中位列第四位,市场份额约3.6%,并且随着更多的多联多价疫苗以及新型疫苗陆续上市,未来全球疫苗市场的增长潜力巨大,预测2026年全球疫苗市场规模将达到561亿美元,年复合增长率约8.1%。
2020-11-18 来源:火石创造 -
 2020年第三季度中国血液制品行业及细分产品市场竞争格局分析
2020年第三季度中国血液制品行业及细分产品市场竞争格局分析2019年年底暴发的新冠疫情,带来了对静丙等治疗性血液制品的大量需求,对恢复期血浆以及静丙、白蛋白等治疗性血制品的宣传,有利于教育医生和民众认识血制品;随着国外疫情持续,进口白蛋白企业采浆受限,进口白蛋白可能减少,加之疫情期间国内采浆量的减少,使得后续白蛋白供应可能下降,国产白蛋白有较强提价预期。
2020-11-17 来源:前瞻经济学人 -
 皮下注射PD-L1抗体KN035提交中国新药上市申请
皮下注射PD-L1抗体KN035提交中国新药上市申请11月16日,康宁杰瑞发布新闻稿,其与思路迪医药(3D Medicines)、先声药业达成战略合作的重组人源化PD-L1单域抗体(研发代号:KN035;通用名:恩沃利单抗注射液)的生物制品上市许可申请(BLA),已正式提交给中国国家药品监督管理局(NMPA)审批。
2020-11-17 来源:医药观澜 -
 新出台的《生物安全法》 对生物医药行业影响究竟有多大?
新出台的《生物安全法》 对生物医药行业影响究竟有多大?10月17日,十三届全国人大常委会第二十二次会议17日表决通过了《中华人民共和国生物安全法》(下文简称“生物安全法”),该法律将从2021年4月15日起施行。
2020-11-16 来源:火石创造










